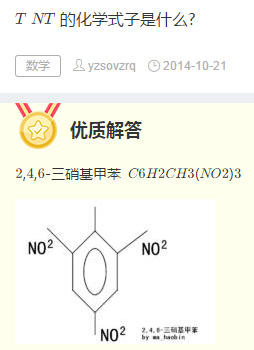
次氯酸的电离方程式
纯净的氯气通入水中时,会形成盐酸和次氯酸:
Cl2 + H2O HCl + HClOKW=1.56×10-4
一氧化二氯溶於水会转变为次氯酸核帆:
Cl2O + H2O 2HClO
次氯酸,化学式为HClO,是种不稳定弱酸,仅能存在於溶液中,一般用作漂白剂、氧化剂、除臭剂和消毒剂
在水溶液中,次氯酸部分电离为次氯酸根离子(ClO−,也称为「次氯酸盐阴离子」)和氢改蔽雹离子(H+):
HClO H+ + ClO−
次氯酸中性溶液是一种比标准状况下的氯更强的氧化剂:
2 HClO(aq) + 2 H+ + 2 e− Cl2(g) + 2 H2OE=+1.63V
注:标准状况指0℃,标准大气压下次氯酸不稳定,会慢慢发生自身氧化还原反应而分解,降低pH会促进该反应的进行:
{2HClO{=\!=}2HCl+O
2HClO{=\!=}2HCl+O
{3HClO-> 2HCl + HClO3}
{3HClO-> 2HCl + HClO3}}}
次氯酸是一种弱酸,可以和碱发生酸碱中和生成相应的盐和水。例如:
HClO+NaOHNaClO+H2O
含并唯有次氯酸根的盐被称为次氯酸盐。最广为人知的一种家用次氯酸盐消毒剂是次氯酸钠(NaClO)。
次氯酸根离子和次氯酸,到底是哪个有漂白性?
次氯酸,因为次氯酸根离子要在酸性条件下才有强氧化性,例如次氯酸钠没有氧化性。
次氯酸根禅搜只有转化为次氯酸时,才有漂白性.如,固体漂白粉不能漂茄败白,只有溶于水,才能转化生成次氯酸,才有漂白性.
拓展:次氯酸钠是一个强碱弱酸盐,其溶于水时会发生水解反应颤袭颤
NaCLO + H2O ==(可逆)==NaOH + HClO
生成了次氯酸,故能漂白
常见的酸根离子(带化学式)
H2CrO4 铬酸 CrO42- 铬酸根
H2Cr2O7 二铬酸 Cr2O72- 二铬酸根
H3PO4 磷酸 PO43- 磷酸根
H3PO3 亚磷酸 HPO32- 亚磷酸根
H3PO2 次磷酸 H2PO2- 次磷酸根
HClO4 过氯悉宽酸 ClO4- 过氯酸根
HClO3 氯酸 ClO3- 氯酸根
HClO2 亚氯酸 ClO2- 亚氯酸根
HClO 次氯酸 ClO 次氯酸根
H2SO4 硫酸 SO42- 硫改敬酸根
H2SO3 亚硫酸 SO32- 亚硫酸根
HNO3 硝酸 NO3- 硝酸根
HNO2 亚硝酸 NO2- 亚硝酸根
H2CO3 碳酸 CO32- 碳酸根核陆慎
HCN 氢氰酸 CN- 氢氰酸根
H2S 氢硫酸 S2- 氢硫酸根
H2C2O4 草酸 C2O42- 草酸根
HMnO4 过锰酸 MnO4- 过锰酸根
H2MnO4 锰酸 MnO42- 锰酸根
次氯酸的化学性质
一元弱酸,见光分解,次氯酸具有很强的氧化性,能杀死水中的细菌,也能使染料等有机色素褪宽烂色,常做消毒剂和漂白剂。
次氯酸,是一种氯元素的含氧酸,化学式为HClO。
它的物理性质是常温下状态仅存在于水溶液中。水溶液在真空中可浓缩到密度1.282,即浓度40.1%。加热到40℃时即分解,并发扮巧耐生爆炸。颜色由无色到浅黄绿色,有非常刺鼻的气味。
化学性质是具有弱酸性、强氧化性和不稳定性,它能使有色布条、品红褪色,使厅春石蕊溶液变为无色液体。次氯酸不稳定,易分解放出氧气。一般用作漂白剂、氧化剂、除臭剂和消毒剂。
次氯酸根离子化学式
次氯酸根是一种化学用品,有较强的氧化性,可用作漂白剂。
中文名
次氯酸根
特性
都有强的氧化性
用途
可做漂白剂
化磨慧合价
ClO-中Cl为+1价
强氧化性
化合价
次氯酸根 ClO-中的Cl为+1价
强氧化性
次氯酸根离子无论在酸性还是碱性溶液中,都有强的氧化性,次氯酸根离子和常见的还原性离子不可以大量共存。如ClO-和Fe2+ 、S2- 、I-、芹念HS- 、SO32- 、HSO3- 等因为发生氧化还原反应不可以大量共存。
常见的次氯酸盐包括NaClO(漂白剂有效成分)和Ca(ClO)2(漂白粉有效成分),都是很强的氧化剂。而瞎首答且都可以溶于水。
强氧化性,被还原成Cl-或Cl2。可做漂白剂。
扩展资料:
次氯酸钠是一种无机物,化学式为NaClO,是最普通的家庭洗涤中的“氯”漂白剂。其他类似的漂白剂有次氯酸钾、次氯酸锂或次氯酸钙,次溴酸钠或次碘酸钠、含氯的氧化物溶液,氯化的磷酸三钠、三氯异氰尿酸钠或钾等,但在家庭洗涤中通常不使用。通常认为漂白性源于其较强的氧化性。漂白剂是能破坏发色体系或产生一个助色基团的变体。
HCl,HClO,HClO2,HClO3,HClO4有什么分别
1.组成上的分别:
氯化氢(HCl),一个氯化氢分子是由一个氯原子和一个氢原子构成的,是无色有刺激性气味的气体。其水溶液俗称盐酸,学名氢氯酸。相对分子质量为36.46。
次氯酸,一种氯元素的含氧酸,化学式为HClO,结构式H-O-Cl,其中氯元素的化合价为+1价,是氯元素的最低价含氧酸,但其氧化性在氯元素的含氧酸中极强,是氯元素含氧酸中氧化性第二强的酸。
亚氯酸,一种氯元素的含氧酸,化学式为HClO2,结构式为H-O-Cl=O,其中氯元素的化合价为+3价。它的氧化性在各种氯元素的含氧酸中为第一强,酸性比氯酸和高氯酸弱,强于次氯酸,是一种中强酸。
氯酸,化学式为HClO3,是氯元素的含氧酸之一,其中氯的化合价为+5价。它具有强酸性与强氧化性,可用于制取多种氯酸盐,亦可用作氧化剂。帆斗它可由氯酸钡与硫酸反应制取。氯酸水溶液在真空中可浓缩到密度1.282,即浓度40.1%。
高氯酸,无机化合物,六大无机强酸之首,氯的最高价氧化物的水化物。是无色透明的发烟液体。高氯酸在无机含氧酸中酸性最强。
2.物理性质上的唤拆不同:
氯化氢是无色,熔点-114.2℃,沸点-85℃,空气中不燃烧,热稳定,到约1500℃才分解。有窒息性的气味,对上呼吸道有强刺激,对眼、皮肤、黏膜有腐蚀。密度大于空气 ,其水溶液为盐酸,浓盐酸具有挥发性。
摩尔质量:36.4606 g/mol,外观无色吸湿性气体,密度:1.477 g/L(25℃)(气)
相对密度(水=1)1.19
相对蒸气密度(空气=1)1.27
熔点:158.8K(-114.2℃)
沸点:187.9K(-85℃)
溶解性(水):72g/100mL(20℃)(标准压强)
饱和蒸气压(Pa):4225.6(20℃)
次氯酸:
常温下状态:仅存在于水溶液中。水溶液在真空中可浓缩到密度1.282,即浓度40.1%。 加热到40℃时即分解,并发生爆炸。
颜色:无色到浅黄绿(显色有变化是因为反应Cl₂+H₂O=HCIO+HCl是可逆反应,在不同状态下平衡状态也不同,显黄绿色是因为溶有氯气的原因)
气味:有类似氯气的刺激性气味
溶解性(与水的体积比):1:2
亚氯酸:
它的氧化性在各种氯元素的含氧酸中为第一强,酸性比氯酸和高氯酸弱,强于次氯酸,是一种中强酸。它是目前唯一存在的亚卤酸。
同时,它也是氯元素的含氧酸中最不稳定的一种,仅存在于溶液中,室温下极容易分解,温度升高分解加快,在几分钟之内便可分解成氯气、二氧化氯和水。
氯酸:
氯酸易溶于水。水溶液在真空中可浓缩到密度1.282,即浓度40.1%。稀的氯酸溶液是无色的,常温时没有气味,浓溶液呈黄色,有类似硝酸的刺激性气味。密度1.282g/cm³。
高氯酸:
是无色透明的发烟液体。高氯酸在无机含氧酸中酸性最强。可助燃,具强腐蚀性、强刺激性,可致人体灼伤。工业上用于高氯酸盐的制备,人造金刚石提纯
3.化学性质上的区别和轿枣:
氯化氢,腐蚀性的不燃烧气体,与水不反应但易溶于水,空气中常以盐酸烟雾的形式存在。易溶于乙醇和醚,也能溶于其它多种有机物
易溶于水,在25℃和1大气压下,1体积水可溶解503体积的氯化氢气体。干燥氯化氢的化学性质很不活泼。碱金属和碱土金属在氯化氢中可燃烧,钠燃烧时发出亮黄色的火焰:
氯化氢气体溶于水生成盐酸,当药水瓶打开时常与空气中的小水滴形成盐酸酸雾。工业用盐酸常成微黄色,主要是因为三氯化铁的存在。常用氨水来检验盐酸的存在,氨水会与氯化氢反应生成白色的氯化铵微粒。
次氯酸:
弱酸性
次氯酸是一种一元弱酸,25℃时的电离常数为3×10-8Ka。
强氧化性
次氯酸能氧化还原性物质(如Na2SO3,FeCl2,KI,C7H7O4N(石蕊)等),使有色布条、品红褪色,并能使石蕊溶液变为无色液体。如:
Na2SO3 + HClO = Na2SO4 + HCl(强氧化剂制弱氧化剂,弱酸制强酸)
标准状况次氯酸中性溶液是一种比标准状况下的氯更强的氧化剂:
2 HOCl(aq) + 2 H+ 2 e⇌ Cl2(g) + 2 H2O E=+1.63V
注:标准状况指0℃,标准大气压
不稳定性
次氯酸很不稳定,只存在于水溶液中。在光照的条件下,它按下式分解:2HClO=light=2HCl+O₂↑ 。它一般用作漂白剂、氧化剂、除臭剂和消毒剂。
在水溶液中,次氯酸部分电离为次氯酸根ClO-(也称为次氯酸盐阴离子)和氢离子H+。含有次氯酸根的盐被称为次氯酸盐。
当纯净的氯气通入水中时,会形成次氯酸和盐酸:Cl₂ + H₂O =可逆=HClO + HCl。次氯酸也是较弱的含氯酸,盐酸的pH和碱度均低于它。
但有极强的氧化性和漂白作用,它的盐类可用做漂白剂和消毒剂,次氯酸盐中最重要的是钙盐,它是漂白粉(次氯酸钙和碱式氯化钙的混合物)的有效成分。漂白粉可由氯和消石灰反应而制得:
2Ca(OH)₂+2Cl₂=Ca(ClO)₂+CaCl₂+H₂O xCaCl₂+yCa(OH)₂+nH2O==xCaCl₂.yCa(OH)₂.nH2O
在放置漂白粉的地方具有氯的气味,就是因为有一氧化二氯放出的缘故。
浓次氯酸溶液呈淡黄色的原因是因为其不稳定,自发分解:
9HClO====HClO3+4Cl2↑+O2↑+4H2O
产生的Cl2以分子形式溶于水呈淡黄色。
次氯酸在溶液中发生3种形式的分解,它们彼此无关,称为平行反应,即:
1.2HClO =光= 2HCl+O₂↑
2.HClO+HCl =可逆= H₂O+Cl₂↑
3.3HClO =△= 2HCl+HClO₃
在阳光直接作用下,按第一种形式分解;在有脱水物质(如CaCl₂)存在时,按第二种形式分解;加热时特别容易按第三种形式分解。如将氯通入热碱溶液中产物是氯酸盐而不是次氯酸盐:3Cl₂+6KOH=KClO₃+5KCl+3H₂O
一氧化二氯和水作用生成次氯酸:H₂O+Cl₂O=2HClO
氯气与水反应生成次氯酸与盐酸:H₂O+Cl₂=HCl+HClO
将氯气通入混有碳酸钙粉末的水中,次氯酸则积集在溶液中,蒸馏反应混合物,可以收集到稀次氯酸溶液。
2HClO==CaCl₂==Cl₂O↑+H₂O
亚氯酸:
酸性
亚氯酸是一种一元中强酸,电离常数Ka为1.1X10-2。
不稳定性
亚氯酸很不稳定,是最不稳定的氯元素的含氧酸,室温下即分解:
其他
亚氯酸可以与碱发生中和反应,如: 利用此方法生产亚氯酸钠。
氯酸:
强酸性
氯酸是一种强酸,无电离常数。
不稳定性
氯酸在加热至40℃时或在浓度在超过40%时会发生分解,并剧烈爆炸,产物不一:
现象:产生大量气体,爆炸效果与硝酸铵类似。
强氧化性
氯酸有强氧化性(略弱于溴酸但强于碘酸,硫酸),在氯元素的各种含氧酸中为第三,常用作强氧化剂。
它与金属反应一般不生成氢气,浓度较高的氯酸与铜反应,生成二氧化氯气体。
高氯酸:
强氧化剂。与还原性有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。
在室温下分解,加热则爆炸(但市售恒沸高氯酸不混入可燃物则一般不会爆炸)。
无水物与水起猛烈作用而放热。氧化性极强,具有强腐蚀性。
其他信息:室温时氧化活性很弱,但浓热的高氯酸是强氧化剂可与大多数金属包括金,银发生反应将他们氧化,生成对应的高价金属高氯酸盐和水