一、钡的化合价是多少
钡的化合价是正二价,化合价是一种元素的一个原子与其他元素的原子构成的化学键的数量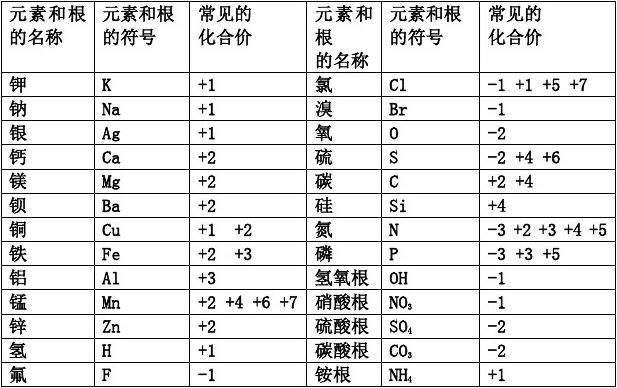 一个原子是由原子核和外围的电子组成的,电子在原子核外围是分层运动的,化合物的各个原子是以和化合价同样多的化合键互相连接在一起的。
一个原子是由原子核和外围的电子组成的,电子在原子核外围是分层运动的,化合物的各个原子是以和化合价同样多的化合键互相连接在一起的。
元素周围的价电子形成价键,单价原子可以形成一个共价键,双价原子可形成两个σ键或一个σ键加一个π键。化合价是物质中的原子得失的电子数或共用电子对偏移的数目。化合价也是元素在形成化合物时表现出的一种性质。
二、钾、锌、铝、钙、钡、镁、铜、铜、锰、硅、硫、氧、氯它们分别的化合价是什么?
钾是+1价
锌钙钡都属于第ⅡA族,价态都显+2价
Al是+3价
Cu由于是副族元素,他会有两个价态:+1价、+2价,当铜显+1价时称为亚铜
锰也是副族,化合价有多种:+2价(MnCl₂)、+3价(Mn₂O₃)、+4价(MnO₂)、+6价(K₂MnO₄)、+7价(KMnO₄)
硅大部分化合物显+4价,少数化合物如SiH₄显-4价
氧元素通常是-2价,而过氧化物如Na₂O₂,则是显-1价。(像O₂F₂显+1价,OF₂显+2价,不过这些东西老师说到大学才学,忽视他们把),还有一些价态是分数形势,如超氧化物、臭氧化物,这些同样不考,也忽视把。
硫显-2价(Na₂S)、作为与氧同族的元素,他的化合价只多不少,你就重点记-2价、+4价(SO₂)、+6价(H₂SO₄)、深点的话还有Na₂S₂O₃,S显+2价
氯通常是-1价,同样有+1价(HClO)、+5价(HClO₃)、+7价的高氯酸
三、常见元素的所有化合价是什么?
常见元素的所有化合价是元素(或原子团)的化合价等于元素原子(或原子团)的电子转移量(包括得失或偏移)。
常见元素的所有化合价有:
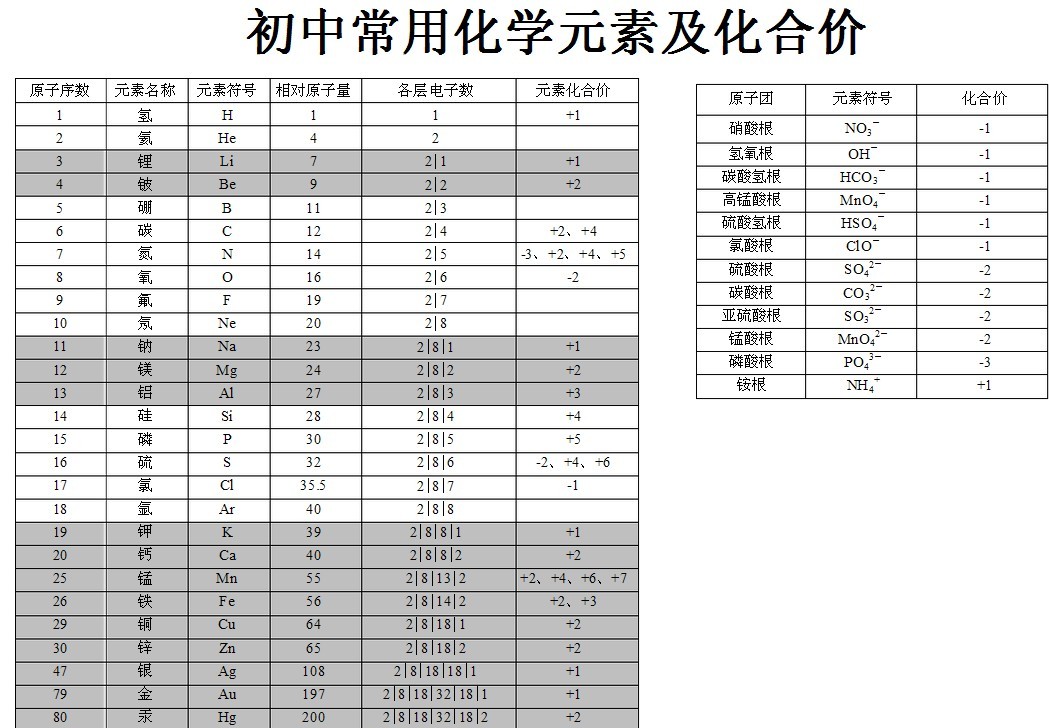
1.钾 K +1 氯 Cl -1,+1,+5,+7
2.钠 Na +1 氧 O -2,-1
3.银 Ag +1 硫 S -2,+4,+6
4.钙 Ca +2 碳 C +2,+4
5.镁 Mg +2 硅 Si +4
6.钡 Ba +2 氮 N -3,+2,+3,+4,+5
7.锌 Zn +2 磷 P -3,+3,+5
8.铜 Cu +1,+2 硫酸根 SO4 -2
9.铁 Fe +2,+3, 碳酸根 CO3 -2
10.铝 Al +3 硝酸根 NO3 -1
11.锰 Mn +2,+4,+6,+7 氢氧根 OH -1
12.氢 H +1 铵根 NH4 +1
13.氟 F -1 磷酸根 PO4 -3 氯酸根 ClO3 -1(Cl +5价)
顺口溜:
钾钠氢银正一价;钙镁钡锌铜正二价。
铝是正三氧负二;铁有正二正三价。
硫有负二正四六;磷有正五正负三。
正一五七负一氯;大家一定要记熟。
四、化学常用元素的化合价都是什么?
氢正一,氧负二,银锂钠钾正一价,锌镁钙钡正二价,铝正三,硅正四,只遇金属或是氢(重中之重务必切记),氟氯溴碘总负一,氮磷负三,硫负二。可变价,不可怕
具体判断和为零(重点),单质为零要记清(牢记,莫忘,注意),亚铜正一铜正二,亚铁正二铁正三
置换反应铁正二,复分解时价不变。
备注:“只遇金属或是氢”化合物中必须有金属元素或氢元素,口诀通用
五、所有化学元素化合价
元素名称 元素符号 常见的化合价 元素名称 元素符号 常见的化合价
钾 K +1 氯 Cl -1,+1,+5,+7
钠 Na +1 氧 O -2
银 Ag +1 硫 S -2,+4,+6
钙 Ca +2 碳 C +2,+4
镁 Mg +2 硅 Si +4
钡 Be +2 氮 N -3,+2,+4,+5
锌 Zn +2 磷 P -3,+3,+5
铜 Cu +1,+2 硫酸根 SO42- -2
铁 Fe +2,+3, 碳酸根 CO32- -2
铝 Al +3 硝酸根 NO3- -1
锰 Mn +2,+4,+6,+7 氢氧化根 OH- -1
氢 H +1 铵根 NH4+ +1
氟 F -1 磷酸根 PO43- -3
硫酸根等根后紧接数字为角码